Aus der barometrischen Höhenformel erhält man
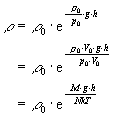
mit der Masse ![]() (m: Molekülmasse).
(m: Molekülmasse).
Die Teilchenzahldichte ![]() ist abhängig von der Höhe h:
ist abhängig von der Höhe h:
![]()
Mit der potenziellen Energie eines Teilchens der Masse m im Gravitationsfeld
![]() ergibt
sich eine Gleichung, die gleichzeitig die Energieverteilung der Teilchen angibt:
ergibt
sich eine Gleichung, die gleichzeitig die Energieverteilung der Teilchen angibt:
![]()
Diese Verteilung lässt sich verallgemeinern:
![]()
Dabei geben g1 bzw. g2 das statistische Gewicht des Zustandes 1 bzw. 2 an.
Bezeichnungen: kT ist die thermische Energie und
![]()
Boltzmann-Faktor
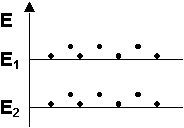 |
Angenommen, es gibt zwei Zustände unterschiedlicher Energien ![]() für n Teilchen. Die Teilchen können sich nur in diesen beiden
Zuständen aufhalten. Dann gilt für das Verhältnis der Teilchenzahlen
n1 und n2 in beiden Zuständen im thermodynamischen
Gleichgewicht
für n Teilchen. Die Teilchen können sich nur in diesen beiden
Zuständen aufhalten. Dann gilt für das Verhältnis der Teilchenzahlen
n1 und n2 in beiden Zuständen im thermodynamischen
Gleichgewicht
![]()
![]() :
:
Ist die thermische Energie kT viel größer als die Energiedifferenz
der beiden Zustände, dann geht der Boltzmann-Faktor gegen 1 und
![]()
![]() :
:
Ist dagegen die thermische Energie viel kleiner als die Energiedifferenz, so
ist der höhere Zustand kaum besetzt und es gilt
![]()
Im thermodynamischen Gleichgewicht tritt der Fall ![]() nicht auf!
nicht auf!
Angenommen, es gibt verschiedene Zustände mit unterschiedlichen Energien Ei. Für die Wahrscheinlichkeit pi, dass ein Zustand i mit Teilchen besetzt ist, gilt
![]() .
.
Die Proportionalität gilt nur, wenn alle Energiezustände gleiche Besetzungsmöglichkeiten haben. Andernfalls muss zusätzlich das jeweilige statistische Gewicht gi der Zustände berücksichtigt werden:
![]()
10 siehe auch Hering (1992, Kap. 3.2.3, S. 154)
© Universität Würzburg, Tilo Hemmert 2000