Die zur Temperaturmessung verwendeten Skalen sind willkürlich festgelegt. Man legt eine lineare Skala zwischen zwei Temperaturfixpunkte, die leicht zu reproduzieren sind.
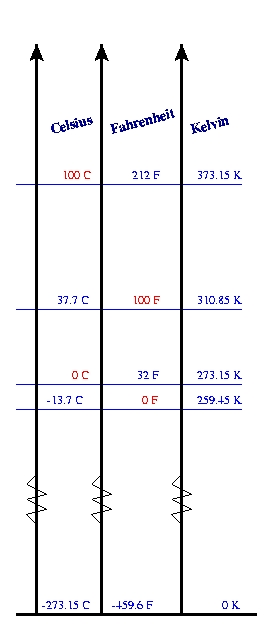 |
| Vergleich der drei Temperaturskalen |
Die bei uns gebräuchliche Celsius-Skala
verwendete ursprünglich den Schmelzpunkt des Eises und den Siedepunkt des
Wasser als Fixpunkte. Anders Celsius (1701-1744) teilte 1742 bei einem Quecksilberthermometer
den Bereich zwischen diesen beiden Fixpunkten in 100 gleich große Skalenteile.
Heute verwendet man anstatt des Schmelzpunktes den Tripelpunkt von Wasser ![]() .
.
Die Fahrenheit-Skala
ist eine andere gebräuchliche Temperaturskala. Daniel Gabriel Fahrenheit
(1686-1732) verwendete den Schmelzpunkt einer definierten Eis-Wasser-Amoniumchlorid-Kältemischung
(![]() ;
; ![]() )
sowie die normale Körpertemperatur (
)
sowie die normale Körpertemperatur (![]() ;
;
![]() ) als Fixpunkte
seiner Skala.
) als Fixpunkte
seiner Skala.
Für die Umrechnung gilt:
![]()
![]()
Umrechnung Celsius - Fahrenheit
0°C = 32°F; 100°C = 212°F
Die von Celsius und Fahrenheit verwendeten Quecksilberthermometer beruhen auf der linearen Ausdehnung des Quecksilbers in einer Glasröhre. Da sich das Glas mit steigernder Temperatur auch selbst ausdehnt, verwendet man für genauere Messungen Gasthermometer.
Die bisher betrachteten Temperaturdefinitionen sind abhängig vom Stoff (Wasser, Eis, Blut, Kältemischung, ...). Im Gegensatz dazu stellt die nach Lord Kelvin benannte Skala eine absolute Temperaturskala dar. Ihr Nullpunkt T = 0 K stellt den absoluten Temperaturnullpunkt dar, d.h. es gibt keine tieferen Temperaturen.
Für die Umrechnung gilt:
![]()
![]()
Umrechnung Celsius - Kelvin
Über das Gesetz von Gay-Lussac gelangt man zum absoluten Nullpunkt (T=0K).
Bei einem Gasthermometer mit idealem Gas hängt der Druck p bei konstantem Volumen V direkt proportional von der Temperatur T ab. Der Proportionalitätsfaktor lässt sich experimentell bestimmen. Damit erhält man das Gesetz von Charles:
![]()
Gesetz von Charles
Analog erhält man bei konstantem Druck
![]()
Gesetz von Gay-Lussac
Dabei sind p0 bzw. V0 der Druck bzw. das
Volumen am Eispunkt ![]() und
und ![]() die
Temperatur in °C.
die
Temperatur in °C.
.gif) |
| Qualitative V(T)-Abhängigkeit verschiedener Gase mit Extrapolation auf den absoluten Nullpunkt. |
Da sich bei tiefen Temperaturen alle Gase aufgrund der intermolekularen Anziehungskräfte
verflüssigen, können Gasthermometer nach unten nur bis zu bestimmten
Temperaturen verwendet werden. Extrapoliert man das Gay-Lussac-Gesetz über
seine Grenzen hinaus, so findet man ![]() als untere Grenztemperatur, die nicht unterschritten werden kann, da sonst V<0
würde.
als untere Grenztemperatur, die nicht unterschritten werden kann, da sonst V<0
würde.
Diesen absoluten Nullpunkt ![]() verwendet man als Ausgangspunkt der Kelvin-Skala, die die gleiche Skaleneinteilung
wie die Celsiusskala hat, d.h. der Temperaturdifferenz von 1 K entspricht 1
°C.
verwendet man als Ausgangspunkt der Kelvin-Skala, die die gleiche Skaleneinteilung
wie die Celsiusskala hat, d.h. der Temperaturdifferenz von 1 K entspricht 1
°C.
Gewöhnlich wird der Buchstabe T verwendet, wenn es sich um Temperaturangaben
in Kelvin (absolute Temperatur) handelt. ![]() (oder
TC) geben Temperaturen in Celsius an.
(oder
TC) geben Temperaturen in Celsius an.
Thermodynamische Funktionen sind in der Regel auf die Temperatur T in Kelvin bezogen!
© Universität Würzburg, Tilo Hemmert 2000